近日,深圳大学医学部生物医学工程学院黄鹏特聘教授团队在美国化学会创办的国际顶级学术期刊《ACS Nano》(影响因子14.588,中科院JCR 1区,TOP期刊)上发表了题为《Tumor-Specific Activatable Nanocarriers with Gas-Generation and Signal Amplification Capabilities for Tumor Theranostics》的文章。这篇文章的所有工作均在深圳大学完成,该团队漆超博士后、何津硕士研究生和付连花副研究员为共同第一作者,黄鹏教授为通讯作者,深圳大学为唯一单位和唯一通信单位,该团队所在的生物医学工程学科属于广东省优势重点学科。
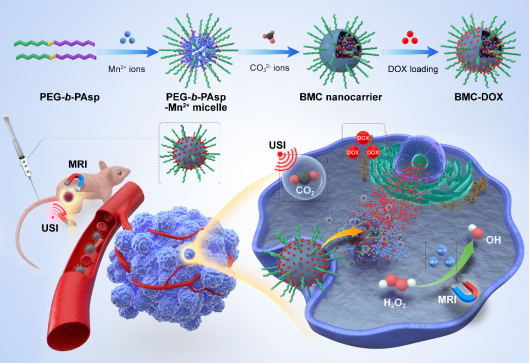
多功能纳米诊疗剂集诊断、治疗、以及疗效监测于一体,可实现个性化的精确诊断和高效治疗。然而,传统纳米诊疗剂通常是通过集成多种功能组分来设计。该策略不仅增加了材料制备过程的复杂性,而且由于各组分在代谢过程中潜在的毒副作用严重阻碍了它们在临床中的应用。为了克服传统多功能纳米诊疗剂存在的缺点,黄鹏教授团队利用聚天冬氨酸(PEG-b-PAsp)为模板,采用原位仿生矿化策略成功制备出碳酸锰矿化的纳米载体(BMC)。该纳米载体具有较高的生物安全性以及肿瘤特异性响应能力,并在酸性肿瘤微环境中分解释放Mn2+离子和CO2气体。其中,释放的Mn2+离子不仅用于肿瘤磁共振成像监测治疗过程,而且通过Mn2+离子介导的化学动力学治疗增强肿瘤治疗效果;释放的CO2气体则用于肿瘤超声成像。此外,BMC对抗癌药物阿霉素(DOX)表现出较高的装载能力以及pH响应的释放特性。体外细胞实验结果表明,DOX负载的BMC对乳腺癌细胞具有较好的杀伤效果,并且体内动物实验也验证了BMC-DOX具有较好的抑瘤效果。因此,这种组成简单且生物可降解的BMC纳米载体,具有肿瘤特异性激活的特点,具有巨大的临床转化前景。
本研究工作得到了国家重点研发计划,国家自然科学基金,广东省自然科学基金、深圳市科创委等项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.0c09223
